《廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展若幹規定(試行)》業經市人民(mín)政府同意,現印發給你們,請認真組織實施。實施中(zhōng)遇到的問題,請徑向市發展改革委反映。
廣州市人民(mín)政府辦(bàn)公(gōng)廳
2018年3月22日
廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展若幹規定(試行)
第一條 為(wèi)貫徹落實《廣州市戰略性新(xīn)興産(chǎn)業第十三個五年發展規劃》和《廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展實施意見》,提升我市産(chǎn)業政策協同水平和綜合競争力,集中(zhōng)資源促進生物(wù)醫(yī)藥産(chǎn)業高端化、規模化、集約化發展,打造全球生物(wù)醫(yī)藥産(chǎn)業重鎮,制定本規定。
第二條 本規定适用(yòng)于在本市進行工(gōng)商(shāng)注冊、稅務(wù)(民(mín)政)登記,從事生物(wù)制藥、化學(xué)藥物(wù)、現代中(zhōng)藥、醫(yī)療器械、醫(yī)用(yòng)材料等領域的研發、生産(chǎn)、流通、服務(wù)等生産(chǎn)經營活動的财務(wù)制度健全、實行獨立核算的獨立法人企業和機構。
第三條 對自主研發及在本市轉化的生物(wù)制品、1—6類中(zhōng)藥、化學(xué)藥品,分(fēn)類改革前申請注冊的1—4類及第5類(僅限靶向制劑、緩釋制劑、控釋制劑)化學(xué)藥品或改革後申請注冊的1—2類化學(xué)藥品分(fēn)階段給予資金扶持,臨床前研究階段的項目優先列入市科(kē)技(jì )計劃;進入臨床I、II、III期研究的新(xīn)藥項目,分(fēn)别給予50萬元、100萬元和200萬元經費扶持。對本市企業取得第二類、第三類醫(yī)療器械産(chǎn)品首次注冊證書的,每個産(chǎn)品首次注冊證書分(fēn)别給予20萬元、50萬元的獎勵。(牽頭單位:市科(kē)技(jì )創新(xīn)委,配合單位:市食品藥品監管局、衛生計生委、财政局)
第四條 支持藥物(wù)非臨床安(ān)全性評價機構(GLP)、藥物(wù)(含醫(yī)療器械)臨床試驗機構(GCP)、有(yǒu)特殊專業要求的臨床研究醫(yī)院、生物(wù)醫(yī)藥産(chǎn)業中(zhōng)試及生産(chǎn)平台等重要公(gōng)共服務(wù)平台項目建設,補助額度不超過項目總投資的30%,單個項目不超過1000萬元。對特别重大的關鍵核心平台項目,采取“一事一議”原則給予特殊優惠扶持。(牽頭單位:市發展改革委,配合單位:市科(kē)技(jì )創新(xīn)委、食品藥品監管局、衛生計生委、财政局)
第五條 對通過國(guó)家GLP、GCP資格認證的本市生物(wù)醫(yī)藥企業和機構給予一次性獎勵,首次獲得藥物(wù)GLP認證批件的認證項目達到3大項以上、6大項以上、9大項以上(均含本數)的,分(fēn)别給予100萬元、200萬元、400萬元獎勵;首次獲得GCP認定證書的,按每通過1個專業給予10萬元獎勵并予以累計(含非首次獲得GCP認定證書的新(xīn)增專業)。對首次獲得國(guó)際AAALAC認證、世界衛生組織(WHO)FERCAP/SIDCER認證、美國(guó)AAHRPP認證的本市生物(wù)醫(yī)藥企業和機構給予一次性200萬元獎勵。(牽頭單位:市科(kē)技(jì )創新(xīn)委,配合單位:市食品藥品監管局、衛生計生委、财政局)
第六條 對本地GLP、GCP、委托合同研究機構(CRO)、生物(wù)醫(yī)藥産(chǎn)業中(zhōng)試平台等研發服務(wù)機構,為(wèi)與本研發服務(wù)機構無投資關系的本市生物(wù)醫(yī)藥企業提供服務(wù)的,按年度合同金額及發票依據的5%給予獎勵,最高不超過500萬元。(牽頭單位:市科(kē)技(jì )創新(xīn)委,配合單位:市食品藥品監管局、衛生計生委、财政局)
第七條 支持企業開展仿制藥質(zhì)量和療效一緻性評價,對本市按國(guó)家規定通過仿制藥一緻性評價基本藥物(wù)目錄内的口服固體(tǐ)制劑品種、以及率先在全國(guó)前三名(míng)通過仿制藥一緻性評價的其他(tā)化學(xué)藥制劑品種,每品種給予200萬元的資金支持。(牽頭單位:市工(gōng)業和信息化委,配合單位:市财政局、食品藥品監管局、發展改革委)
第八條 對獲得美國(guó)食品藥品監督管理(lǐ)局(FDA)、歐洲藥品管理(lǐ)局(EMEA)、世界衛生組織(WHO)等國(guó)際先進體(tǐ)系認證的項目優先列入市重點技(jì )術改造項目,按照最高不超過項目投資額30%給予支持。(牽頭單位:市工(gōng)業和信息化委,配合單位:市食品藥品監管局、科(kē)技(jì )創新(xīn)委、财政局)
第九條 對獲得新(xīn)藥證書的新(xīn)藥(含原料藥、創新(xīn)輔料等)以及獲得注冊或備案的中(zhōng)藥配方顆粒、創新(xīn)醫(yī)療器械和優先審批醫(yī)療器械,在本市實現産(chǎn)業化的項目,按項目總投資的30%給予後補助支持,最高不超過400萬元。(牽頭單位:市發展改革委,配合單位:市财政局、科(kē)技(jì )創新(xīn)委、衛生計生委、食品藥品監管局)
第十條 鼓勵和支持生物(wù)醫(yī)藥企業在本市建設生産(chǎn)廠房和辦(bàn)公(gōng)用(yòng)房,意向用(yòng)地優先納入市、區(qū)年度土地利用(yòng)計劃,保障用(yòng)地指标。對本市生物(wù)醫(yī)藥産(chǎn)業項目實行工(gōng)業用(yòng)地先租賃後出讓、彈性年期出讓制度。工(gōng)業用(yòng)地使用(yòng)權租賃權年限不超過10年,彈性年期出讓的土地使用(yòng)權出讓年限不超過30年。對特别重大項目,采取“一事一議”的原則确定優惠地價。(牽頭單位:市國(guó)土規劃委;配合單位:各區(qū)政府,市城市更新(xīn)局、發展改革委)
第十一條 推進生物(wù)醫(yī)藥企業循環化改造,園區(qū)開展集中(zhōng)供熱、土地集約利用(yòng)、企業間廢物(wù)交換利用(yòng)、水的循環利用(yòng)等,将危險廢棄物(wù)、固體(tǐ)廢物(wù)集中(zhōng)處理(lǐ)納入園區(qū)配套工(gōng)程。對處理(lǐ)園區(qū)内生物(wù)醫(yī)藥企業“危廢”的專業機構,給予每噸處置費用(yòng)500元,最高不超過100萬元的補貼。(牽頭單位:市環保局、工(gōng)業和信息化委,各區(qū)政府;配合單位:市财政局)
第十二條 對于常年需要進行科(kē)研、臨床研究或生産(chǎn)用(yòng)品(試劑、儀器設備、生物(wù)樣品、抗體(tǐ)原研對照藥等)進出口的生物(wù)醫(yī)藥相關單位,由市科(kē)技(jì )創新(xīn)委建立單位目錄,定期通報海關和檢驗檢疫部門。廣州海關和黃埔海關積極對進入名(míng)錄的企業開展信用(yòng)培育工(gōng)作(zuò),對成為(wèi)海關認證企業的給予相應海關優惠便利。(牽頭單位:廣州海關、黃埔海關、市科(kē)技(jì )創新(xīn)委、廣州檢驗檢疫局,配合單位:市發展改革委、食品藥品監管局)
第十三條 生物(wù)醫(yī)藥領域的諾貝爾獎、拉斯克醫(yī)學(xué)獎獲得者、中(zhōng)國(guó)兩院院士等專家帶項目、技(jì )術和團隊來穗進行産(chǎn)業化的項目,按照項目總投資的10%給予支持,單個項目最高不超過1000萬元。(牽頭單位:市發展改革委,配合單位:市科(kē)技(jì )創新(xīn)委、财政局)
第十四條 支持本市生物(wù)醫(yī)藥企業拓展國(guó)際業務(wù),對國(guó)際業務(wù)額首次達到100萬美元以上,給予10萬元至100萬元人民(mín)币資助,對同一企業補貼最高不超過100萬元人民(mín)币。對本市生物(wù)醫(yī)藥企業的境外非關聯并購(gòu)投資,按照企業上一年度實際彙出投資額(美元絕對值),給予不超過5%的直接資助,最高不超過1000萬元人民(mín)币。支持本市醫(yī)藥企業從境外引進先進技(jì )術到本市産(chǎn)業化或由本市企業主導産(chǎn)業化,給予技(jì )術交易金額的10%資助,最高不超過1000萬元人民(mín)币。(牽頭單位:市商(shāng)務(wù)委,配合單位:市财政局、廣州海關、黃埔海關)
第十五條 設立首期規模100億元的廣州生物(wù)醫(yī)藥産(chǎn)業投資基金,扶持新(xīn)藥、創新(xīn)醫(yī)療器械項目及生物(wù)醫(yī)藥産(chǎn)業園區(qū)建設,被投項目在審評審批、藥品監督管理(lǐ)等方面納入市、區(qū)有(yǒu)關部門綠色通道、優先辦(bàn)理(lǐ)。成立廣州市生物(wù)醫(yī)藥産(chǎn)業聯盟,集合“政産(chǎn)學(xué)研用(yòng)融”等産(chǎn)業資源,構建獨具(jù)特色的生物(wù)醫(yī)藥産(chǎn)業生态圈。組建高層次顧問專家智庫,為(wèi)産(chǎn)業發展提供決策咨詢。自聯盟成立之日起連續3年,每年劃撥專項經費50萬元,用(yòng)于支持開展技(jì )術創新(xīn)協作(zuò)、交流活動、組織培訓及舉辦(bàn)高端論壇、展會等大型活動。(牽頭單位:市發展改革委,配合單位:市财政局、工(gōng)業和信息化委、科(kē)技(jì )創新(xīn)委、衛生計生委、食品藥品監管局、金融局、民(mín)政局)
第十六條 申請單位或個人應對提交所有(yǒu)材料的真實性作(zuò)出書面承諾。市、區(qū)有(yǒu)關部門将對失信企業、機構和個人實施聯合懲戒,依法在信用(yòng)工(gōng)作(zuò)門戶網站和行業網站、報刊、廣播、電(diàn)視等媒體(tǐ)上集中(zhōng)公(gōng)示相關信息,依法依規采取行政性約束和懲戒措施。
第十七條 本規定自印發之日起施行,有(yǒu)效期3年。
附件:廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展若幹規定操作(zuò)指南(試行)
附件
廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展若幹規定操作(zuò)指南(試行)
一、根據《廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展若幹規定(試行)》(以下簡稱《若幹規定》),為(wèi)進一步規範管理(lǐ),制定本操作(zuò)指南。
二、《若幹規定》和本指南所稱生物(wù)醫(yī)藥産(chǎn)業是指《廣州市加快生物(wù)醫(yī)藥産(chǎn)業發展實施意見》中(zhōng)生物(wù)醫(yī)藥、高端醫(yī)療器械相關領域,包括幹細胞與再生醫(yī)學(xué)、精(jīng)準醫(yī)療、基因檢測、高端醫(yī)療等新(xīn)興領域。
三、市生物(wù)醫(yī)藥産(chǎn)業發展領導小(xiǎo)組辦(bàn)公(gōng)室負責落實《若幹規定》中(zhōng)規定的各類獎勵、補助或補貼資金。由各牽頭單位會同市财政局分(fēn)項組織項目申報及編制年度資金預算。各牽頭單位組織認定、管理(lǐ)和監督。市、區(qū)有(yǒu)關部門各司其職、密切配合,建立聯動機制,制定配套措施,增強服務(wù)意識,打造醫(yī)藥産(chǎn)業發展“綠色通道”,合力開創我市生物(wù)醫(yī)藥産(chǎn)業發展新(xīn)局面。
四、申請《若幹規定》支持的單位(以下簡稱申請單位),應同時具(jù)備如下條件:在廣州市注冊經營并依法納稅,有(yǒu)實際經營場所,具(jù)有(yǒu)獨立法人資格和規範的财務(wù)核算制度,各項經營指标納入廣州市相關統計範圍,無違法及不誠信行為(wèi)。
五、申請單位須提交資金申請報告、三證(五證)合一的營業執照、信用(yòng)記錄、上一年度财務(wù)審計報告複印件等基本材料,并應根據各條款要求提交以下材料,經審核通過後獲得支持。
(一)第三條規定的申請單位應提供:相關注冊批件或證書。
(二)第四條規定的申請單位應提供:平台項目備案/核準、土地/房産(chǎn)、規劃、環評等文(wén)件,主要人員簡介、服務(wù)設施、軟件或設備儀器清單、平台管理(lǐ)辦(bàn)法和規章制度、自有(yǒu)資金證明和貸款承諾等材料。其中(zhōng)GLP機構建設标準為(wèi):國(guó)家食品藥品監管部門頒發的GLP認證批件中(zhōng)有(yǒu)關試驗項目不少于六大項。
(三)第五條規定的申請單位應提供:相關批件或證書。
(四)第六條規定的申請單位應提供:收費标準、經公(gōng)證後的服務(wù)合同及發票依據,工(gōng)商(shāng)部門出具(jù)的股權結構證明等材料。
(五)第七條規定的申請單位應提供:通過一緻性評價的相關批件或證明。
(六)第八條規定的申請單位應提供:相關批件或證書、市重點技(jì )術改造項目要求的材料。
(七)第九條規定的申請單位應提供:相關注冊批件或新(xīn)藥證書、生産(chǎn)批件及GMP認證、項目備案/核準、生産(chǎn)場所資質(zhì)、環評等文(wén)件,主要人員名(míng)單、設備儀器清單、自有(yǒu)資金證明和貸款承諾等材料。
(八)第十條規定的申請單位應提供:項目用(yòng)地審批文(wén)件、不動産(chǎn)産(chǎn)權證明、租賃合同等材料。
(九)第十一條規定的申請單位應提供:危險廢物(wù)經營許可(kě)證、危險廢物(wù)處理(lǐ)合同、危險廢物(wù)轉移聯單及有(yǒu)關票據。
(十)第十二條規定的申請單位應提供:産(chǎn)品研發(含臨床試驗)合同及票據、臨床研究報告等材料。
(十一)第十三條規定的申請單位應提供:團隊主要人員身份及榮譽證明,項目相關性的專家意見、項目備案/核準、生産(chǎn)場所資質(zhì)、環評等文(wén)件,設備儀器清單、自有(yǒu)資金證明和貸款承諾等材料。
(十二)第十四條規定的申請單位應提供:銷售合同、銷售發票、收彙憑證、并購(gòu)合同、付款憑證、技(jì )術進口合同、技(jì )術進口合同登記證書、技(jì )術進口合同數據表等證明材料。
六、相關批件和證書等文(wén)件原則上以申報時間一年内獲批的為(wèi)準,具(jù)體(tǐ)由各有(yǒu)關部門在發布申報指南時予以進一步明确。
七、《若幹規定》提到的貨币單位如未注明的均以人民(mín)币計算,涉及“不超過”“以上”的數額均含本數。具(jù)體(tǐ)内容如與我市其他(tā)扶持政策交疊,按照“就高不重複”原則處理(lǐ)。各項規定政策由牽頭部門統一受理(lǐ),涉及的各類獎勵、補助、補貼等資金的使用(yòng)和管理(lǐ)按照市有(yǒu)關規定執行。各部門原則上不再另行制定生物(wù)醫(yī)藥專項政策(現有(yǒu)政策除外)。
附件:1.申請材料真實性聲明
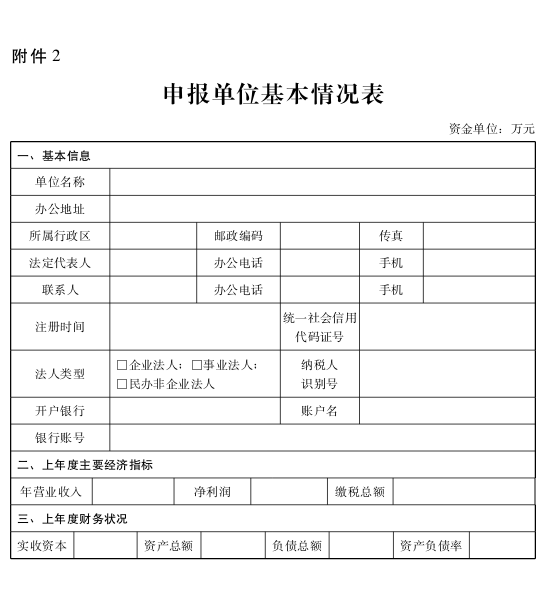
2.申報單位基本情況表

廣州市人民(mín)政府辦(bàn)公(gōng)廳秘書處 2018年3月27日印發






